|
|
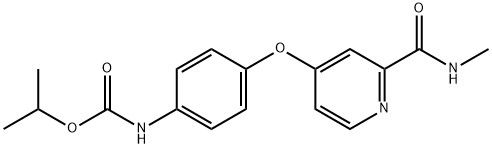
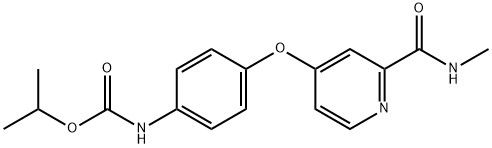
95+ Polvere bianca Sorafenib Impurità D CAS 2206827-14-5
|
Dettagli:
Termini di pagamento e spedizione:
|
| Nome del prodotto: | Sorafenib Impurità D | Numero CAS: | 2206827-14-5 |
|---|---|---|---|
| M.W.: | 329.35 | MF: | C17H19N3O4 |
| Apparizione: | Polvere bianca | Purezza: | 95+ |
| EINECS No: | - | Immagazzinamento: | 5-25°C |
Descrizione del prodotto
Polvere bianca Sorafenib Impurità D CAS 2206827-14-5 95+
Nome:Impurità D di regorafenib
CAS NO:2206827-14-5
M.W.329.35
Apparizione: Polvere bianca
Purezza: 95+
Sinonimi:Impurità D di regorafenib
Applicazione
Regorafenib Impurità D è un' impurità specifica presente nel Regorafenib, un farmaco utilizzato principalmente nel trattamento di alcuni tipi di cancro come inibitore della multi-cinasi.quando si tratta dell' applicazione di Regorafenib Impurità D, non serve come principio attivo per scopi terapeutici.
Infatti, le impurità dei farmaci sono fattori che richiedono un controllo rigoroso durante la produzione farmaceutica per garantire la sicurezza e l'efficacia del farmaco.Alte concentrazioni di impurità possono potenzialmente influenzare la purezza, la stabilità e l'attività biologica del farmaco, portando ad effetti negativi o a benefici terapeutici ridotti.Il controllo delle impurità è un passo cruciale nello sviluppo e nella produzione di farmaci..
Lo studio di Regorafenib Impurità D si concentra sulla comprensione delle sue proprietà chimiche, delle sue potenziali attività biologiche e dei meccanismi di formazione durante la produzione e lo stoccaggio del farmaco.Conducendo ricerche approfondite su questa impurità, le aziende farmaceutiche possono ottimizzare i loro processi di produzione, ridurre i livelli di impurità e, in ultima analisi, migliorare la qualità e la sicurezza del prodotto finale.
Pacco
![]()
![]()
![]()
![]()
Trasporti
I piccoli pacchi ((1g, 25g, 1Kg, 25Kg) possono essere spediti via Express. (DHL, FedEx, EMS, ecc.)
I pacchi di grandi dimensioni ((100 kg e più di100 kg) possono essere trasportati via aerea o via mare.
Tutti i trasporti sono in accordo con le esigenze del cliente.
Profilo aziendale
![]()
![]()
![]()
![]()
![]()
![]()
Persona di contatto: admin
-
98+ Impurità della polvere bianca ((Standardi) 6-Chloro-N-Methylpyridine-2-Carboxamide CAS 845306-04-9
-
98+ Polvere bianca TICAGRELOR CAS 1129683-88-0 C14H14N4O3
-
98+ Impurità della polvere bianca ((Standardi) Impurità del sorafenib 16 CAS 2206827-12-3
-
98+ Polvere bianca Sorafenib Composto correlato 8 NO. 1431697-81-2 CAS
-
98+ Polvere bianca Sorafenib Impurità 6 CAS 1285533-84-7
-
Puro 98+ bianco in polvere Sorafenib Impurità 3 CAS NO. 284670-98-0 C27H24N6O5